Правило фаз (хим.). — Неоднородность любой химической системы, находящейся в равновесии, может обуславливаться только одновременным присутствием в ней различных однородных тел, взаимно соприкасающихся; таков, напр., случай твердой соли и находящегося над ней насыщенного раствора и т. д. Отдельные, однородные тела, из которых сложена система, могут быть в газообразном, жидком или твердом состояниях; число твердых тел и число взаимно не растворяющихся жидкостей, которые принимают участие в равновесии, не подлежит какому-либо ограничению; что касается паро- или газообразных тел, то благодаря способности их смешиваться во всех отношениях, паро- или газообразный комплекс, входящий в систему, должен быть всегда в единственном числе. Гиббс предложил называть фазами те физически и химически однородные массы (иначе, массы однородной концентрации), из которых сложенаданная неоднородная равновесная система. Фазами могут быть потому и физич. смеси, и химически однородные тела; число их, следовательно, не всегда совпадает с числом химических тел, которые могут быть выделены из данной системы; так, всякий раствор, будет ли он твердый (см. Растворы), жидкий или газообразный, представляет собой отдельную фазу, за химические же тела (простые или сложные), ее образующие, мы должны принимать исключительно те, концентрация которых может быть произвольно изменена. Напр., при рассмотрении равновесия между углекальциевой солью, окисью кальция и углекислым газом, за тела, слагающие данную систему мы должны принять CO₂ и СаО, потому что их концентрация может быть произвольно изменяема и их двух вполне достаточно для образования всех тут возможных равновесных систем (ср., что сказано ниже при двух реагирующих телах); нельзя принять за слагающие сами элементы кальций, кислород и углерод, так как они не представляют независимых переменных и, что не менее важно — не находятся в равновесии с данной системой [1]. Гиббсу (Gibbs) принадлежит положение, что в системах, находящихся под равномерным влиянием тяготения, электрического, капиллярного или какого-либо иного натяжения, — состояние фаз определяется: давлением и температурой системы и химическими потенциалами тел, из которых она (система) сложена. При равновесии — потенциал данного тела, находящегося в различных фазах, обладает определенной постоянной величиной, и потому: 1) для любой фазы мы можем составить уравнение, которое будет связывать эти величины между собой, и 2) для каждой другой фазы, находящейся в равновесии с первой, будем иметь такого же вида уравнение, содержащее те же переменные. Несмотря на то, что неизвестны ни эти отдельные уравнения, ни химические потенциалы участвующих в данной системе тел, все же эти соображения позволили Гиббсу вывести вполне определенные заключения о характере и числе возможных случаев равновесия при неизвестном числе тел, участвующих в образовании системы. Действительно, число независимых переменных для n тел, по определению равно «n + 2» (n химических потенциалов + температура + давление), а следовательно, число теоретических уравнений равно числу переменных только при наличности «n + 2» фаз; это число фаз является, кроме того, максимальным для n не зависимых друг от друга химических тел. Только в этом случае все переменные имеют вполне определенное численное значение, иначе говоря, сосуществование «n + 2» фаз влечет за собой определенное соотношение между температурой и давлением; такие системы, не обладающие степенью свободы (Рике), Тревор называет безвариантными (nonvariant system). Если условиться откладывать температуры по оси абсцисс прямоугольных координат, а по оси ординат — давления, то в плоскости координат всегда можно найти такую точку, которая будет изображать состояние системы, сложенной из n тел и имеющей «n + 2» фаз; эту точку принято называть «инверсионной», или «точкой обращения» (Фан’т-Гофф). Когда при n реагирующих телах имеется налицо только «n + 2» фаз, то число неизвестных превышает на единицу число уравнений, которые можно для нее построить, и система оказывается обладающей одной степенью свободы, моновариантной (по Тревору — monovariant system); для такой системы величина одной из переменных, или температуры, или давления, может быть произвольно выбрана; ряду данных температур будут в ней отвечать вполне определенные давления, и наоборот, определенные давления возможны будут только при определенных температурах; в диаграмме температур и давлений такой системе будет отвечать уже не точка, а кривая линия. Если представить себе, что из сосуществующих при инверсионной точке «n + 2» фаз по очереди будет исчезать какая-нибудь из них, то, очевидно, мы получим в координатной плоскости «n + 2» кривых, которые все будут пересекаться при «точке обращения». Система из n тел, образованная n фазами, называется дивариантной (divariant system); две переменные могут быть в ней заранее выбраны, и в диаграмме температур и давлений такой системе отвечает определенная площадь, границы которой определяются кривыми моновариантных систем. В дивариантной системе при данной температуре можно иметь (при соответственных изменениях концентраций) целый ряд давлений; при данном давлении температура может меняться в зависимости от концентрации, или наоборот, концентрация может меняться с изменением температуры и т. д. Наконец, системы из n слагаемых (реагирующих тел), состоящия из n − 1, n − 2 и т. д. фаз называются три-, тетравариантными и т. д. (trivariant, tetravariant system); число степеней свободы, очевидно, возрастает по мере увеличения числа реагирующих тел, сравнительно с числом фаз; на практике иcследование три- и т. д. вариантных систем не представляет интереса благодаря их малой определенности и слишком большому числу возможных комбинаций. Системы, обнимаемые П. фаз, подчинены, как равновесные, общему закону Ле-Шателье, по которому, «всякие изменения внешних факторов равновесия влекут за собой обратные изменения внутри системы» (см. Обратимость химических реакций), а именно: 1) нарастание температуры вызывает в системе превращение (физическое или химическое), стремящееся понизить температуру, поглощающее, следовательно, тепло, и обратно, и 2) всякое увеличение внешнего давления вызывает такое перемещение равновесия, которое влечет за собой понижение давления, состоящее, следовательно, в уменьшении объема системы, и обратно. Следующие частные случаи наглядно поясняют вышеизложенное.


![Фиг. 4.[2]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/69/Brockhaus_and_Efron_Encyclopedic_Dictionary_b48_855-2.jpg/180px-Brockhaus_and_Efron_Encyclopedic_Dictionary_b48_855-2.jpg)

I. Одно реагирующее тело (вода, бензол, сера, фосфор). При одном реагирующем теле (т. е. при n = 1) максимальное число для сосуществующих фаз равно 1 + 2 = 3; это число, отвечающее безвариантной системе, возможно только при температуре и давлении, отвечающих инверсионной точке; при всяких же других величинах температуры и давления могут сосуществовать уже maximum n + 1, т. е. 2 фазы. В диаграмме температур и давлений инверсионная точка должна представлять точку пересечения трех пограничных кривых для трех возможных моновариантных систем. Фиг. 1, схематически изображающая равновесие для воды в ее различных физических видоизменениях, все это ясно показывает. А есть инверсионная точка, в которой может одновременно существовать вода в трех видах (фазах): вода газообразная (вернее, парообразная), вода жидкая и твердая (лед). Температура, отвечающая ей = + 0,0075 °C, а давление = 4,57 мм (см. Вода и Лед). Стоит хотя бы незначительно изменить или температуру, или давление, чтобы тотчас вызвать вполне определенное превращение в системе, состоящее в исчезновении одной из фаз. Так, если мы будем уменьшать температуру системы, то исчезнет жидкая вода и останется система из льда и пара; давление испаряющегося льда будет меняться — падать с падением температуры, но так как лед может существовать (ниже точки А) при различных температурах и давлениях, то, очевидно, равновесие между ним и паром должно выражаться кривой АО (фиг. 1); экспериментально она прослежена для очень малого участка температур, теоретические же соображения заставляют предполагать, что эта кривая должна кончаться в нулевой точке координат, т. е. при абсолютном нуле температуры (при −273 °C, Нернст); это обозначено пунктиром. Кривая ОА есть вместе с тем кривая возгонки льда (ср. Пар) или максимального его давления. Диаграмма ясно показывает, что если при постоянной температуре над системой из льда и пара уменьшать давление, то этого нельзя сделать, пока еще остается хоть небольшое количество льда, и только после полного испарения его давление может быть понижено; и наоборот, повышение давления невозможно, пока еще над льдом данной температуры имеется пространство, наполненное паром. Если повышать температуру системы (выше инверсионной точки А), то должна исчезнуть фаза льда, и рассуждениями, вполне подобными только что изложенным, нетрудно прийти к выводу, что кривая АС есть кривая максимальной упругости паров воды в присутствии жидкой воды, т. е. так называемых насыщенных паров (см. Вода). Ниже нее лежит область пара ненасыщенного или перегретого (см. Вода), непосредственно выше — область жидкой воды. Относительно пограничных точек кривой АС надо заметить следующее. Как показано пунктиром, она может быть экспериментально прослежена на некотором расстоянии ниже точки А, где кривая DA отвечает упругости переохлажденной воды (ср. Лед и Пар), но современные сведения не позволяют решить, отвечает ли ее конец какому-нибудь определенному физическому изменению воды, или же кривая точно так же должна окончиться в нулевой точке координат (Нернст), т. е. не должна ли диаграмма иметь вид, представленный на фиг. 2. Справа кривая АСимеет, напротив, вполне твердо установленное окончание, и именно абсцисса точки Спредставляет так называемую критическую температуру воды, а ее ордината давление при критической температуре, т. е. 365° и 200 атм. (Кальете и Колардо). При температурах выше критической жидкая вода исчезает, превращаясь нацело в газообразную; моновариантная система (вода + насыщенный пар) сменяется, следовательно, дивариантной (критическая точка та, при которой две фазы становятся тождественными; Гиббс, Оствальд), для которой могут быть по произволу выбраны величины давления и температуры, что и показано расходящимися из точки С пунктирными прямыми (фиг. 1), которые изображают наблюденные Кальете и Колардо давления газообразной воды в зависимости от количества ее, подвергавшегося нагреванию; прямой ход их показывает, что и при этих высоких температурах и давлениях газообразная вода еще довольно близко следует закону Гей-Люссака для расширения газов. Может ли быть газ переохлажден ниже критической температуры и будет ли он тогда обладать каким-нибудь определенным давлением, — до сих пор не решенный вопрос; согласно П. фаз величины температуры и давления в однородных, дивариантных системах могут быть выбраны по произволу, а ход кривой при данной массе вещества находится в зависимости от его концентрации, т. е. от объема, занятого им [3]. С кривыми ОА и AC в точке А пересекается еще третья кривая АВ; она отвечает равновесию между льдом и водой при отсутствии газообразной фазы, следовательно, под давлением. Как видно по нанесенной пунктиром вертикальной линии NN1N2, кривая AB отклоняется влево, что происходит потому, что лед обладает меньшим уд. весом, чем вода, и с увеличением давления температура плавления льда понижается (кривая, благодаря уменьшению абсциссы, должна приближаться к оси y-ов). Пунктирные прямые ММ1М2 и NN1N2, из которых первая параллельна оси х-ов, а вторая оси у-ов, легко позволяют ориентироваться в тех изменениях, которым должна подвергаться исследуемая система в одном случае при изменении только температуры (след., при постоянном давлении), а в другом при изменении давления (при постоянной температуре); ясно, что если при постоянном давлении понижать температуру газообразной (парообразной) воды, то, пока температура не понизится до М1, будут иметься налицо условия моновариантной системы; в точке M2 она превратится в безвариантную (жидкость + определенное давление + насыщенный пар), затем снова в моновариантную (отрезок М1М2 отвечает жидкой воде + определенному давлению), которая в M2 становится безвариантной (жидкая вода + лед + определенное давление) и т. д. В точках М1 и М2 как нетрудно видеть, должны происходить остановки в ходе температуры до полного исчезновения в M1 газообразной фазы, а в M2 — жидкой. Одинаково понятно, что на прямой NN1N2 должно встретиться две особых точки в N1 и N2, в которых давление не может возрастать, пока не исчезнет в N1 — газо-(паро)-образная фаза, а в N2 — твердая (лед). В большинстве случаев соответственные диаграммы для других тел, способных существовать в различных физических состояниях, отличаются от диаграммы фиг. 1 в том отношении, что благодаря большему (сравнительно с жидкостью) уд. весу твердых тел при точке плавления, кривая моновариантной системы (твердое тело + жидкое) отклоняется вправо от оси у-ов, а не влево. Фиг. 3 отвечает этому случаю; так, например, для бензола точка A лежит при 5,58° (Ферхе) при давлении его пара в 36,06 мм ртутного столба, точка С при 288,5 °C и давлении в 47,5 атмосфер (Юнг, Рамзей), а кривая AB отклоняется вправо и приблизительно на 0,03° при увеличении давления на одну атмосферу (при 4,92 атм. точка плавления бензола повысилась на 0,143°; Ферхе). Явление усложняется при возможности аллотропических (см. Изомерия) форм. Пока неизвестны тела, для которых существовали бы две жидких фазы, но для порядочного числа тел найдены два и более твердых видоизменения. Это влечет за собой возможность существования, кроме точки плавления, еше других инверсионных точек. Такова, напр., сера. Для нее с несомненностью (Митчерлих) установлены два аллотропических видоизменения: сера, так называемая октаэдрическая, кристаллизующаяся октаэдрами ромбической системы, и сера призматическая, являющаяся в виде вытянутых призм одноклиномерной системы. Фиг. 4 представляет схематически наблюдаемые тут равновесные системы. При обыкновенной температуре, ромбическая сера является более устойчивым видоизменением и кривая аО представляет собой кривую ее возгонки, аС есть кривая упругости насыщенного пара жидкой серы и, наконец, аВ — кривая, отвечающая моновариантной системе: ромбическая сера + жидкая. Инверсионная точка a (точка плавления ромбической серы) лежит при 114,5° (Броди). При 120° лежит другая инверсионная точка А1, отвечающая плавлению одноклиномерной серы; в ней сосуществуют: сера одноклиномерная (площадь АА1В), сера жидкая (площадь BA1C) и пар серы; кривая АА1 представляет, следовательно, кривую возгонки одноклиномерной серы, а А1В — кривую равновесия одновариантной системы: сера одноклиномерная + жидкая. Третья инверионная точка А обусловливается сосуществованием фаз: сера ромбическая + сера одноклиномерная + пар; она лежит при 95,55° (Рейхер, Фан’т-Гофф), и наконец, четвертая, пока не наблюдавшаяся экспериментально инверсионная точка В может лежать по приблизительному расчету Б. Роозебоома около 131 °C при 400 атмосферах давления. Что касается кривых, отвечающих моновариантным системам, то они до сих пор очень мало изучены. Ниже точки А давление паров серы слишком незначительно, чтобы его было удобно наблюдать. Кривая АА1 не наблюдалась непосредственно. Необходимость отклонения кривой АВвправо следует с несомненностью из того, что уд. вес ромбической серы = 2,07 (Маршаль и Шефер) выше уд. веса одноклиномерной = 1,958 (С. К. Девилль) и что превращение одноклиномерной серы в ромбическую сопровождается выделением тепла (Митчерлих); кроме того, Рейхер прямым опытом установил, что с повышением давления температура равновесия между ромбической и одноклиномерной серой повышается около 0,049 °C на каждую атмосферу давления, так как при 60 атм. точка равновесия находится при 96,2°; выше этой температуры и этого давления кривая не прослежена. Что касается кривой А1В, то ее направление нанесено гадательно на основании некоторых данных, по которым уд. вес жидкой серы меньше уд. веса одноклиномерной. Положение точки B, очевидно, тоже в высшей степени гадательно [4]. Выше нее не может существовать одноклиномерная сера (заиимающая сравнительно ограниченную площадь АВА1; разность между абсциссами точек Аи A1 = 24,45 °C, разность ординат точек Аи В около 400 атм.), а двухфазная система (сера твердая + жидкая) должна быть образована серой ромбической + жидкой серой. В минералогическом отношении это важно потому, что объясняет ход образования кристаллов самородной серы; при обыкновенном давлении из расплавленной серы кристаллизуется одноклиномерная сера, а при давлениях выше 400 атм. даже и без переохлаждения могла бы получаться ромбическая (Фан’т-Гофф). Наблюдаемые на опыте явления не совсем так просты, как они только что изложены, и усложнение обуславливается главным образом тем, что превращения ромбической серы в одноклиномерную и обратно происходят не мгновенно, а требуют, напротив, довольно значительного промежутка времени, благодаря чему можно наблюдать, напр., точку плавления октаэдрической серы, лежащую в области одноклиномерной серы (см. фиг. 4), а во-вторых, можно иметь и одноклиномерную серу при температурах, лежащих ниже точки А в переохлажденном состоянии; прибавка кристаллика октаэдрической серы (Жернез) или даже незначительного количества какого-нибудь растворителя серы (Митчерлих) очень способствует устранению явлений переохлаждения. Кроме нанесенных на диаграмме 4 кривых, отвечающих более твердо установленным аллотропическим видоизменениям серы, на ней должна бы еще быть нанесена кривая, изображающая упругость пара твердой серы, не растворимой в сероуглероде. Ход этой кривой до сих пор не установлен экспериментально; насколько можно думать, по имеющимся до сих пор наблюдениям (Бертело, Девиль, Жернез), кривая эта должна пересекать кривую ОА где-то около точки А (может быть выше нее) и затем при температурах около 250° пересекать линию А1С; в точках пересечения будут, очевидно, иметься условия для безвариантных систем. Яснее эти отношения установлены для фосфора, относительно которого мы ограничиваемся только схематической диаграммой, данной Банкрофтом (фиг. 5). ЕА — кривая возгонки твердого белого фосфора, AC — кривая упругости насыщенного пара жидкого фосфора; пунктирное продолжение AC — упругость паров переохлажденного жидкого фосфора; другая пунктирная линия из А отвечает моновариантной системе: фосфор твердый + фосфор жидкий; кривая BD — кривая давления паров красного фосфора. Несмотря на неустойчивое равновесие, белый фосфор не переходит сам собой в красный. Как видно, во всех случаях, согласно требованию теории, во всех инверсионных точках имеются по три фазы. И наоборот, определение числа сосуществующих фаз позволяет решить, сколько независимых переменных принимают участие в равновесии; необходимо только, чтобы на системе не сказывалось влияние тяготения, капиллярных сил и т. д. (см. выше), а чтобы изучение ее велось при давлениях и температурах, свойственных самой системе, потому что наличность какого-нибудь определенного давления или определенной температуры, как было указано при обсуждении диаграммы для воды, понижает степень свободы системы, превращая дивариантную в моновариантную, а моновариантную в безвариантную, что влечет за собой нахождение ложных инверсионных точек.

![Фиг. 8. Фиг. 9.[5]](http://upload.wikimedia.org/wikipedia/commons/thumb/7/70/Brockhaus_and_Efron_Encyclopedic_Dictionary_b48_858-0.jpg/300px-Brockhaus_and_Efron_Encyclopedic_Dictionary_b48_858-0.jpg)



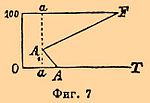
II. Два реагирующих тела. При двух реагирующих телах максимальное число фаз равно 4-м; три фазы образуют моновариантную систему и т. д. Можно различить, по-видимому, два типа, смотря по тому, отсутствует между фазами жидкая фаза или же она имеется налицо. Первый случай (отсутствие жидкой фазы) тесно примыкает к только что разобранным явлениям перемены однородными телами физического состояния. Если пар (или газ), выделяемый данной твердой однородной системой, отличается от нее по химическому составу, то, очевидно, что часть ее претерпевает химическое разложение, продуктами которого являются выделяемый газ и некоторый остаток; газ и остаток являются, таким образом, теми телами, теми независимыми переменными (см. что сказано выше о разложения СаСО3), из которых может быть построена исходная система. Пока она не вся распалась, мы имеем дело с тремя фазами: исходная система + газ + остаток, иначе говоря — с моновариантной системой, и в ней определенной температуре должно отвечать определенное давление и наоборот, как, напр., при испарении жидкостей. Аналогия идет дальше и в том, что величина давления (при данной температуре) не зависит от отношения между массами неразложенной системы и твердого продукта распада ее. Сюда могут быть отнесены: диссоциация исландского шпата на окись кальция и углекислоту (Дебрэ, Ле-Шателье; см. Диссоциация, X, 664), диссоциация солей, с кристаллизационной водой (Дебрэ, Видеман, Лекёр и др.) или кристаллизационным аммиаком (Изамбер) и т. д. (см. X, 666). Во втором случае, когда присутствует жидкая фаза, изменение давления (при постоянной температуре) влечет за собой изменение равновесия, а вместе с тем изменение относительного состава одной (или нескольких) фаз. Представим себе воду при постоянной темп.; достаточно незначительно уменьшить давление, чтобы заставить ее до конца испариться; явление резко меняется, когда в ней растворена какая-нибудь соль, что, как известно, влечет за собой понижение давления пара в зависимости от концентрации соли; если над таким раствором уменьшить на какую-нибудь небольшую, но определенную величину давление, то испарится (при постоянной температуре) уже не вся вода, а только часть ее, и это потому, что по мере испарения воды возрастает концентрация соля и соответственно падает упругость пара раствора; испарение, очевидно, прекратится, когда она (упругость) сравняется с данным давлением. Таким образом состояние равновесия систем, заключающих фазы переменного состава (растворы), находится в зависимости от относительных количеств реагирующих тел в этих фазах, или, иначе, от их концентраций. Эти последние измеряются гораздо легче давлений пара растворов, и потому мы будем пользоваться тут и диаграммами, в которых ординатами будут не давления, а концентрации. Следующие примеры поясняют сказанное. Пусть дан раствор азотнокислого серебра в воде. Четыре фазы в этом случае: твердое AgNO3, лед, раствор и парообразная Н2О [6]; сосуществование их обуславливает безвариантность системы, которой на диаграмме температур и давлений (фиг. 6) отвечает точка А1; в ней, как видно, пересекаются четыре кривых, отвечающих четырем возможным моновариантным системам. Кривая ОА1 отвечает одновременному присутствию: твердой соли, льда и пара Н2О; согласно опытам Реньо, который нашел, что присутствие твердой соли не влияет заметным образом на упругость пара льда, мы должны считать эту кривую тождественной с кривой ОА фиг. 1. Кривая A1MF отвечает одновременнному присутствию твердой соли, раствора и пара воды, т. е. отвечает упругости пара, так называемых, насыщенных растворов AgNO3 в воде; с возвышением температуры, как видно, кривая быстро поднимается кверху, переходит через максимум (М), после которого наступает быстрое падение ее; под конец она падает вертикально (Б. Роозебоом), пересекая ось х-ов при температуре плавления безводной AgNO3 (+198 °C), при каковой температуре AgNO3 смешивается во всех отношениях с водой (растворимость AgNO3 в воде при этой температуре безгранично велика). Кривая А1В1 отвечает одновременному присутствию льда, AgNO3 и раствора; экспериментально она не изучена; можно только сказать, что она должна отклоняться влево, потому что система из льда и твердой соли удельно легче жидкой системы того же состава. Каждая из площадей чертежа имеет вполне определенное значение; площадь ОА1MF дает условия сосуществования AgNO3 и пара Н2О, площадь ОА1B1 — AgNO3 и льда; В1А1М — для AgNO3 и раствора. Точка А1 есть криогидратная точка, т. е. такая, при которой раствор нацело застывает, распадаясь на AgNO3 и лед, но только криогидратная точка не под атмосферным давлением, а под максимальным давлением упругости насыщенного при этой температуре раствора AgNO3. Пока мы имели дело только с насыщенными растворами при разных температурах и разных давлениях. Для того, чтобы диаграмма обнимала собой растворы любой концентрации (до чистой воды, как предела уменьшения концентрации), необходимо соединить фиг. 6 с фиг. 1-й. Благодаря неизменяемости упругости пара льда от присутствия соли — при наложении этих чертежей друг на друга кривые ОА1 (фиг. 6) и ОА (фиг. 1) должны до температуры, отвечающей точке А1 (фиг. 6), совпасть между собой; в силу того же самого кривая А1А(фиг. 6), отвечающая сосуществованию льда, раствора и пара воды должна тоже совпасть с линией ОА (фиг. 1). Точки А, В и С (фиг. 6) представляют собой соответственные точки фиг. 1, и следовательно, площадь ВАСпо-прежнему отвечает чистой жидкой воде, а пограничные кривые AB и АС показывают условия превращения воды в твердое (лед) и паро-(газо)-образное состояние. Плошадь CAA1MF обнимает собой область ненасыщенных растворов и пара; она ограничена кривыми: A1MF насыщенных растворов, АС — воды и А1А кривой точек плавления льда (выделяемого растворами). Площадь BAA1B1 отвечает области сосуществования ненасыщенных растворов и льда; границами ее являются: А1 В1 — кривая криогидратных точек (при давлениях больших, чем давление пара криогидратного раствора в точке А1), AB — кривая понижающихся точек плавления льда с возрастанием давления и кривая А1А. Диаграмма ясно показывает: 1) что наименьшей упругостью пара обладают (при любой температуре) насыщенные растворы (см. Растворы); 2) что по мере разжижения их водой (уменьшения концентрации растворенного, нелетучего вешества) упругость их возрастает, приближаясь к упругости пара чистой воды, взятой при той же температуре; 3) что температура выделения из раствора льда (кривая А1А) понижается с увеличением концентрации растворенного тела и 4) температура кипения (образования пара определенного давления, равного внешнему давлению, под которым находится система) одновременно возрастает [7]; — но она не дает представления о том, как меняется концентрация насыщенных растворов, а потому естественным дополнением ее служит концентрационно [8] температурная диаграмма. Этар нашел, что с повышением температуры азотнокислое серебро растворяется все в меньшем количестве воды и при 198 °C (точка плавления AgNO3) становится способным смешиваться с водой во всех отношениях. Если по оси у-ов прямоугольных коорданат откладывать величины концентрации растворов AgNO3, a по оси х-ов температуры, то, очевидно, кривая [9] растворимости AgNO3 должна с повышением температуры, идя слева направо, подниматься и максимальной темп. (абсциссе) 198 °C. должна отвечать ордината F (фиг. 7), равная, по условию, 100 (см. примечание). С понижением температуры концентрация раствора падает; следовательно, из него должна выделяться растворенная соль; процесс выпадения AgNO3 продолжается до тех пор, пока одновременно с солью не начинает выпадать и лед, т. е., пока температура насыщенного раствора не достигнет криогидратной (A1), или в данном случае — 6,5 °C. Если пробовать уменьшать еще концентрацию соли, то за криогидратной точкой при охлаждении раствора первым будет выпадать в твердом виде лед (раствор будет не насыщен по отношению к AgNO3), и кроме того по мере уменьшения концентрации раствора температура образования в нем льда (температура замерзания его должна приближаться к + 0,0075 °C (см. выше), а следовательно, кривая от точки A1 должна, падая, идти слева направо и пересекать ось х-ов (при значении ординаты = 0) в + 0,0075 °C. Очевидно, кривые AA1 и FA1 являются не только кривыми растворимости, но в то же время они дают и точки плавления: AA1 льда при возрастающей концентрации AgNO3, a FA1 — азотнокислой соли в присутствии увеличивающегося количества воды; точка пересечения A1 представляет наинизшую температуру, которой можно достигнуть смешением AgNO3 со льдом. Площадь FA1A обнимает собой все ненасыщенные растворы и отвечает площади FMA1AC фиг. 6; площадь OaA1a 100 отвечает площади OA1B1 фиг. 6, линия A1F изображает состав насыщенных растворов в присутствии пара воды, которым в фиг. 6 отвечала кривая A1MF; точка A1 — четвертая точка безвариантной системы, линия A1A представляет состав растворов при одновременном присутствии льда и пара и, след., отвечает моновариантной системе AA1 фиг. 6. Таким образом, очевидно, что обе фиг. могут быть представлены, как проекция одна другой; это и сделано на фиг. 8 [10]. Как и все предыдущие, она тоже является схематической. Явления несколько усложняются, когда растворенная в воде соль способна образовать с ней химически определенные гидраты. Фиг. 9 представляет схематический чертеж зависимости между температурой, давлением и концентрациями для водных растворов сернонатриевой соли, которая, смотря по условиям опыта, может выпадать из раствора или в виде Nа2SO4, или Na2SO4.10H2O, или же Na2SO4.7H2O. Значение кривых OA1A, A1B1,A1C1 то же самое, что в фиг. 6 (вместо А1C1 там A1M), с той разницей, что растворенным телом является в данном случае не AgNO3, a Na2SO4.10H2O. Если моновариантную систему из Na2SO4.10H2O, насыщенного раствора и пара нагревать, то в точке С1 наблюдается образование новой фазы, так как из раствора при температуре, отвечающей C1, начинает выпадать безводная соль. Образуется, след., новая безвариантная система, состоящая из Na2SO4, Na2SO4.10H2O, раствора и пара и способная существовать, пока не исчезнет вся десятиводная соль, после чего остается новая моновариантная система: Na2SO4, раствор и пар, которой и отвечает кривая С1С2. В точке C1 таким образом пересекаются две кривых А1С1 и C1C2; последняя поднимается круче первой потому, что выше точки С1 падает концентрация раствора, благодаря уменьшению растворимости Na2SO4 с повышением температуры. Вообще, всякий раз, когда при данной температуре растворенная соль претерпевает какое-нибудь изменение, — растворимость продукта изменения выше этой температуры должна быть меньше растворимости неизмененной соли (Ле Шателье, Фан’т-Гофф) [11], что связано с поглощением тепла при всяких процессах, обусловленных повышением темп. (закон Ле-Шателье). Линия ОС3С1 есть продолжение С1С2 Температурно-концентрационная диаграмма (схематическая) на той же фиг. 9 показывает, что обеим безвариантным системам отвечают изменения в направлении кривых концентрации. Что касается кривой А2С3 отвечает семиводному гидрату; на верхней половине диаграммы она нанесена пунктиром потому, что упругость пара насыщенных растворов этой соли не изучена; судя по тому, что Na2SO4.7H2O образуется при температуре ок. 26 °C (Левель), лежащей ниже температуры точки C1 (32,6°; Фан’т-Гофф) и при безвариантной точке С3 существуют одновременно: Na2SO4 , Na2SO4.7H2O-раствор и пар, то надо думать, что упругость пара насыщенных растворов Na2SO4.7Н2О меньше упругости пара насыщенных (при тех же температурах) растворов Na2SO4.10H2O. Могут ли обе соли быть в равновесии друг с другом, неизвестно и пока мало вероятно. Судя по диаграмме, это если возможно, то только вблизи криогидратной точки. Некоторые соли (CaCl2, Fe2Cl4) образуют соединения с кристаллизационной водой, плавящиеся без разложения (Б. Роозебоом); для выяснения наблюдаемых явлений достаточно остановиться на растворах CaCl2.6H2O. Если, начиная с криогидратной темп. (т. е. с −55 °C) состав безвариантной системы (лед, твердый СаСl2.6Н2О, раствор и пар) прибавлять к раствору CaCl2, то можно увеличивать концентрацию CaCl2 до тех пор, пока раствор не будет иметь состава СаСl2.6Н2О, тогда он нацело плавится при 30,2°С [12]. Замечательно, что дальнейшее прибавление СаСl2 дает раствор, выделяющий при охлаждении в некотором промежутке концентраций снова шестиводный гидрат; таким образом возможны два насыщенных раствора CaCl2.6H2O: один содержит CaCl2 меньше приведенной формулы, а другой больше, и воды в нем меньше 6 молекул на каждую молекулу CaCl2; последний, как более концентрированный, выделяет СаСl2.6Н2О при более низких давлениях сравнительно с первым; стоек он только на протяжении одного градуса, так как уже при 29,2 °C из него начинают выпадать кристаллы СаСl2.4Н2Оβ. Возможность подобной пары растворов вполне понятна, если принять во внимание, что, раз СаСl2.6Н2О способен плавиться без разложения, то точка плавления его (или, что то же, температура выпадения его из раствора) должна понижаться как от прибавки воды, так и от прибавки CaCl2, с той лишь разницей, что прибавка воды должна вызывать увеличение давления водяного пара (т. е. газообразной фазы), а прибавка CaCl2, наоборот — уменьшать его. По аналогии с теми явлениями, которые наблюдаются для растворов AgNO3, можно даже предвидеть до известной степени ход изменения давления пара раствора с приближением к темп. 30,2 °C, а именно должно перед этой точкой для растворов, содержащих CaCl2 менее СаСl2.6Н2О, ожидать максимума упругости, а затем в точке плавления CaCl2.6H2O вертикального ее падения; для растворов, более богатых CaCl2, надо ожидать, что кривая упругости, являющаяся вначале продолжением предыдущей (Б. Роозебоом, Лоренц, Фан’т-Гоффт) [13] довольно быстро будет падать, отклоняясь влево. Фиг. 10 (схематическая) показывает, что опыт вполне отвечает предвидению теории. Начиная с криогидратной точки А1 (состав фаз см. выше), кривая упругости моновариантной системы — CaCl2.6H2O + раствор + пар — быстро растет, достигает в M максимума (= 7,02 мм при 28,5 °C), вертикально падает в точке F (t = 30,2°, р = 6,699 мм), а в точке Н1, отвечающей безвариантной системе: СаСl2.6Н2О + СаСl2.4Н2Оβ + раствор + пар, она пересекается с кривой упругости OF сухой СаСl2.6Н2О (Фан’т-Гофф). Нижняя темп.-концентрационная часть диаграммы дополняет верхнюю; значение букв в ней то же, что и в фиг. 7, 8 и 9, так что она не требует дальнейших пояснений. Остальные гидраты СаС2 (Б. Роозебоом установил еще существование гидратов CaCl2.4H2O α, CaCl2.2H2O и CaCI2.H2O) повторяют явления, наблюдаемые для CaCl2.6Н2О. В общем ходе их растворимости такой, какой предвидится на основании законности Ле-Шателье (Фан’т-Гоффа) и может быть выражен схематически диаграммой фиг. 11, построенной подобно предыдущим концентрационно-температурным диаграммам. А — точка плавления растворителя; А1 — криогидратная точка, обусловленная системой: лед + [соль + (m + n)Н2О] + раствор + пар; А1 А2 — концентрации при различных температурах моновариантной системы: [соль + (m + n)Н2О] + раствор + пар; А2 точка перелома, благодаря появлению безвариантной системы: [соль + (m + n)Н2О) + [соль + n Н2О] + раствор + пар; А2А3 — кривая моновариантной системы: [соль + n Н2О] + раствор + пар и т. д. В инверсионных точках угловые коэффициенты кривых растворимости при переходе от высшего гидрата к низшему уменьшаются и касательные к кривым в точкак пересечения перемещаются (при данном положении диаграммы) по направлении часовой стрелки [14]. К растворам CaCl2 тесно примыкают, по общему характеру, явления, наблюдаемые при взаимодействии хлора и йода. А именно, Стортенбекер нашел, что если в расплавленный треххлористый йод JCl2 (темп. пл. 101 °C F фиг. 12; р = 16 атм.) вносить J, то, по мере образования однохлористого J и насыщенного раствора JCl3 в JCl (моновариантная система состоит из JCl3 + JCl + пар), давление раствора падает, как показано кривой FE. В точке Е (t = 22,7°, р = 42 мм) система превращается в безвариантную, благодаря появлению однохлористого йода JClα (фазы JCl3 + JCl α + раствор + пар); при дальнейшем прибавлении йода треххлористый йод исчезает и образуется моновариантная система из JClα + раствор + пар; до точки F1 раствор содержит избыток хлора, а после нее избыток йода сравнительно с формулой JCl, и наблюдаемые явления отвечают разобранным выше для растворов СаСl2.6Н2О. В точке F1 (t = 27,2°, p = 39 мм) JClα плавится. В Е1 (t = 7,9°, p = 11 мм) снова появляется безвариантная система из йода твердого + JСlα + раствор + пар. Дальнейшее прибавление йода влечет за собой исчезновение JClα, и получается моновариантная система: йод + раствор + пар, пределом которой должна быть точка плавления йода (t = 118°); кривая Е1А2 не была прослежена до этой точки, и потому конец ее обозначен пунктиром; пунктиром же нанесены и вероятные давления растворов хлора в треххлористом йоде. Кривая A1MF, отвечающая вероятной моновариантной системе: JCI3 + раствор + пар [15], оканчивается в криогидратной точке А1, где можно ожидать сосуществования: хлора твердого + JCl3 + раствор + пар; кривая ОА2А — есть кривая давления возгоняющегося твердого хлора; точка А отвечает темп. плавления хлора, т. е. — 102° (по Вроблевскому); кривая АС отвечает моновариантной системе: хлор жидкий + газообразный; кривые AB, А1В1, А2В2 и т. д. отвечают моновариантным системам, для которых отсутствуют газообразные фазы; все они экспериментально не изучены. Остается добавить, что кривая E2F2 отвечает изомерному однохлористому йоду JClβ, открытому Траппом; условия равновесия его с системой: JCl3 + раствор + пар Стортенбекером не установлены; точка F2 лежит при 13,9 °C. Что касается температурно-концентрационной диаграммы, то необходимо отметить, что в полном согласии с представлением Ле-Шателье кривые EF1 и F1e1 пересекаются под углом; в остальном диаграмма является повторением фиг. 7, 8 и 10. Перечисленные случаи взаимодействия двух тел наиболее часто наблюдаются. О взаимодействии двух жидкостей, образующих жидкие же фазы, об отношении многих растворов сернокислых солей к нагреванию и об области твердых растворов см. Растворы. Общий вид температурно-концентрационных кривых настолько характерен, что по нему можно судить, каким образом реагирует между собой данная пара тел. Когда они относятся друг к другу как растворители, то наблюдаются только две кривых (фиг. 7); каждая из них начинается точкой плавления соответственного тела (безвариантной системой); затем обе кривых отклоняются влево (ось х-ов температура; ось у-в концентрация), так как они выражают собой понижение точки плавления растворителя (как обыкновенно выражаются) под влиянием растворенного тела; обе кривых сходятся в «криогидратной» точке (см. Криогидрат) в случае водных растворов, или «эвтектичной точке» для других сплавов (преимущественно металлических) [16]. Когда данная пара тел образует одно или несколько химически определенных соединений, не способных плавиться без разложения, то наблюдаются несколько пересекающихся кривых (фиг. 9 и 11), началом которых служат точки плавления взятых веществ, а точки пересечения (из них две эвтектичных) отвечают безвариантным системам. Фиг. 10 и 12 показывают ход кривых при образовании парой реагирующих тел химических соединений, могущих плавиться почти без разложения (кривая AFH фиг. 10), или же вполне стойких (кривая EF1Е1 фиг. 12). На последней диаграмме ясно, что началом кривых и здесь являются точки плавления исходных веществ, образующих равновесную систему; первоначальное направление кривых левое; оно переходит в правое только после «эвтектичных» точек; на ней видно также, что когда пара тел образует сравнительно стойкое химическое соединение, способное плавиться, то точка плавления его обязательно лежит между двумя температурно более низкими инверсионными точками: точка F (фиг. 12) лежит между точками A1 и E, абсциссы которых меньше абциссы точки F, то же самое видно для точек F1 и F2; это явление общее и оно дает твердую руководящую нить при изучении таких случаев взаимодействия двух тел между собой, когда, благодаря их непрозрачности (напр., при сплавах металлов) или благодаря слишком высоким или низким температурам, мы не имеем возможности непосредственно наблюдать происходящие явления (см. подробнее Сплавы). Дальнейшее приложение П. фаз см. Фракционированная перегонка, Фракционированное выпаривание и Фракционированное осаждение.


III. Три реагирующих тела. При трех реагирующих телах безвариантная система должна содержать 5 фаз и в отвечающей ей инверсионной точке должно сходиться 5 кривых, представляющих 5 моновариантных систем, каждая из которых должна в свою очередь содержать по 4 фазы, и т. д. Диаграммы температур и давлений для систем с тремя реагирующими телами не представляют затруднений, и фиг. 13 представляет схематическое изображение одной из таких безвариантных систем. Зато температурно-концентрационные диаграммы на плоскости оказываются невозможными; приходится ограничиться диаграммами, указывающими соотношения между реагирующими телами при какой-нибудь определенной температуре. Если имеем дело с двумя солями и водой, то тогда можно этого достигнуть, относя все растворы к постоянному количеству воды и откладывая по оси х-ов количества одной, а по оси у-ов количества другой из взятых солей (Шрейнемакерс), но безводные соли и системы, содержащие незначительные количества третьего тела, не находят себе места на таких диаграммах. Гораздо удобнее метод, предложенный Левенгерцем и введенный особенно в употребление В. Роозебоомом. Представим себе равносторонний треугольник (фиг. 14), каждая сторона которого разделена на 100 равных частей, и условимся считать, что углы А, В иС отвечают чистым реагирующим телам, и пусть, например, требуется найти точку, отвечающую смеси А, В и С, которая содержит а% 1-го, b% — 2-го и с% третьего тела. Точка А отвечает 100 % А, и чтобы нанести на диаграмму а% А, мы должны отложить от угла В линию, равную а; соответственно от А откладываем линию, равную b; расстояние между ними по условию (а + b + с = 100) будет равно с. Если теперь из точки D провести линию, параллельную ВС, а из Е линию, параллельную АС, то точка пересечения их F и будет представлять собой искомую систему. Чтобы дать более ясное представление о получающихся кривых, фиг. 14 представляет равновесие между тремя жидкостями (водой, хлороформом и уксусной кислотой), исследованное Райтом. Если к механической смеси почти не растворимых друг в друге хлороформа и воды прибавлять понемногу уксусной кислоты, то отдельные слои, на которые была разделена первоначальная система, понемногу уменьшаются благодаря тому, что они начинают взаимно растворяться, и наконец наступает полное смешение их, система становится однородной. Так, при 18 °C. Райтом найдено:
| В нижнем тяжелом слое. | В верхнем легком. | |||||
|---|---|---|---|---|---|---|
| CHCl3 | Н2О | С2Н4О2 | СНСl3 | Н2О | С2Н4О2 | |
| № 1 | 67 % | 5 % | 28 % | 18 % | 31 % | 51 % |
| № 2 | 60 % | 8 % | 32 % | 25 % | 25 % | 50 % |
| № 3 | 56 % | 10 % | 34 % | 29 % | 23 % | 48 % |
и смешание наступило при составе 42 % CHCl3, 16 % Н2О и 42 % С С2Н4О2. Эти данные и были нанесены на диаграмму [17] (В — 100 % СНСl3, С — 100 % H2O); пунктирные линии 1 — 1, 2 — 2, 3 — 3 соединяют соответственные пары сосуществующих растворов; как видно, они не параллельны между собой; точка G отвечает той концентрации, при которой происходит полное смешение. Ниже пунктирной линии 1 — 1 ход кривых схематичный. Как видно, мы имеем дело ниже точки G с двувариантной системой (3 реагирующих тела и 3 фазы: два раствора + пар) и относительные концентрации ее фаз должны меняться с изменением как температуры, так и давления. Наиболее наглядно можно выразить влияние температуры, откладывая ее (т. е. температуру) по оси, перпендикулярной к плоскости чертежа, и строя отвечающие опытным температурам кривые; ряд таких наложенных друг на друга диаграмм дает возможность наглядно выразить состояние системы при различных условиях. Обыкновенно повышение температуры влечет за собой повышение взаимной растворимости реагирующих веществ, и при той температуре, когда происходит их полное смешение, т. е. когда они становятся безгранично растворимыми друг в друге, кривая, очевидно, сливается с очертаниями треугольника; явление может значительно усложниться при низких температурах, особенно, если реагирующие тела образуют между собой химические соединения; подробности надо смотреть в специальных сочинениях. Там же надо смотреть и об условиях равновесия четырех реагирующих тел. Ввиду новизны предмета указываем литературу. Кроме "Thermodynamische Studien W. Gibbs’a (перев. Ostwald’a, Лпц., 1892, стр. 115 и далее) и статей В. Roozeboom’a и его учеников: Schreinemakers’a, Stortenbeker’a, van Rijn van Alkemade, Meyerhoffer’a, помещенных в «Recueil de trav. des Pays-Bas» и в «Zeitschrift für physikalische Сhemie», можно указать: W. Meyerhoffer, «Die Phasenregel und ihre Anwendungen»; W. Bancroft, «The Phase Rule»; van’t Hoff, «Vorlesungen über theoretische und physkalische Chemie» (в этом соч., впрочем, слово «фаза» не встречается и потому оно несколько неясно для начинающего); более краткие очерки: M. Planck’a, в «Grundriss der Thermochemie», W. Nernst’a, в его «Theoretische Chemie» (имеется теперь 2-е издание, которым не удалось воспользоваться при составлении этой статьи), и и во 2-м издании «Allgemeine Chemie», Оствальда (2-я пол. 2-го тома.
Дополнение
[править]Правило Фаз — см. Фаз закон (доп.).
Примечания
[править]- ↑ Paзличиe числа не зависимых друг от друга тел, образующих данную равновесную систему, от числа химических индивидуумов, в ней могущих содержаться, еще яснее выступает на следующем примере. Положим, что в воде растворены одновременно хлористый калий и бромистый натрий, в силу двойного разложения они дадут некоторые количества бромистого калия и хлористого натрия. Нетрудно убедиться, что несмотря на присутствие четырех солей, мы имеем дело всего с тремя независимыми переменными (предполагая концентрацию первоначально взятых солей определенной). Действительно, представим себе, что количества КСl, КВr и NaCl нами установлены, количество неизмененного NaBr, очевидно, будет тем самым косвенно определено; оно не является, следовательно, независимым. К тому же заключению приводит и то соображение, что достаточно в данном случае трех аналитических данных (напр., определений количеств K, Cl, Br), чтобы иметь возможность вычислить четвертое неизвестное (содержание Na, Мейергоффер). Аналогичные соображения позволяют обходиться, не прибегая к теории электролитической диссоциации, при изложении с точки зрения П. фаз случаев равновесия водных растворов солей (Банкрофт).
- ↑ На Фиг. 4 вместо OAAc следует читать OAA1C. (См. Поправки и дополнения к т. XXV. — Прим. ред.).
- ↑ В этом отношении диаграмма, приведенная Банкрофтом в его сочинении «The Phase Rate», является, несомненно, ошибочной.
- ↑ В тексте дана диаграмма Фан’т-Гоффа, допускающего, что точка B лежит ниже 120° Ц.; по Б. Роозебому кривая А1B тоже отклоняется вправо.
- ↑ На Фиг. 9 вместо 00 следует читать 100. (См. Поправки и дополнения к т. XXV. — Прим. ред.).
- ↑ Теоретически можно ожидать, что с паром воды будет и парообразное AgNO3, но на практике мы можем его считать в данных пределах температуры совершенно не летучим.
- ↑ О законах, которым подчинены депрессии упругостей паров растворов, точек замерения их и т. д. — см. Растворы.
- ↑ Под концентрацией соли в данном растворе, согласно Этару, будет подразумеваться количество (весовое) соли в 100 вес. частях раствора (см. Растворы).
- ↑ На самом деле он состоит из двух пересекающихся почти прямых линий. Точка пересечения, лежащая при 55 °C, отвечает температуре аллотропического изменения AgNO3. На фиг. 7 для простоты нанесена одна прямая A1F.
- ↑ Прием введен в употребление Фан’т-Гоффом (см. в конце статьи литературу вопроса).
- ↑ Курнаковым указано, как на исключение, что розео-пентамивовые соли — MX3.5NH3.H2O (где М = Со, Cr, Ir, Ro) более растворимы, чем пурпурео-соли — МХ3.5NН3, но так как активность группы Х в первых солях иная и, кроме того, розео-соли не образуют с пурпурео-солями в растворе равновесных систем, то едва ли можно считать это действительным исключением.
- ↑ Bcякий подобный случай плавления определенного гидрата в растворе, имеющем тожественный с ним состав, вполне аналогичен превращению жидкости при критической температуре в газ, так как оба явления подходят под одно и то же определение; две фазы становятся тожеественными.
- ↑ По Ле-Шателье, обе кривых должны встретиться под углом, это наблюдается, когда соединение, способное плавиться, вполне стойко при температуре плавления (Лоренц).
- ↑ Это находится в связи с тем, что теплота растворения высшего гидрата более соответствующей величины для низшего гидрата или безводной соли (если эти последние могут образоваться при нагревании растворов высших гидратов).
- ↑ Ход кривой не будет отвечать действительности только в случае образования соединения, более богатого хлором, чем JCl3.
- ↑ Оба термина введены Гутри.
- ↑ В диаграмме верхние цифры 1 и 3 надо переставить
